Sindrome da iperstimolazione ovarica: la più temuta complicanza della stimolazione ovarica controllata
La sindrome da iperstimolazione ovarica (OHSS) rappresenta una delle complicanze più temute e potenzialmente pericolose associate ai trattamenti di procreazione medicalmente assistita e alla stimolazione ovarica controllata. Questa condizione sistemica si caratterizza per un aumento significativo della permeabilità vascolare peritoneale, che determina spostamento di fluidi ricchi di proteine dallo spazio intravascolare alle cavità peritoneale e pleurale, causando ascite, idrotorace e potenziali complicanze sistemiche gravi. L'OHSS presenta un'incidenza del 2-6% nelle forme moderate e dello 0,1-0,2% nelle forme severe, con un tasso di mortalità stimato di 1:450.000-500.000 casi. La patogenesi è strettamente correlata all'azione del fattore di crescita endoteliale vascolare (VEGF) stimolato dalla gonadotropina corionica umana (hCG), utilizzata per indurre la maturazione follicolare finale nei cicli di fecondazione assistita. La comprensione dei meccanismi fisiopatologici e delle strategie di prevenzione ha portato allo sviluppo di approcci terapeutici innovativi, incluso l'utilizzo di agonisti del GnRH per il triggering della maturazione ovocitaria.
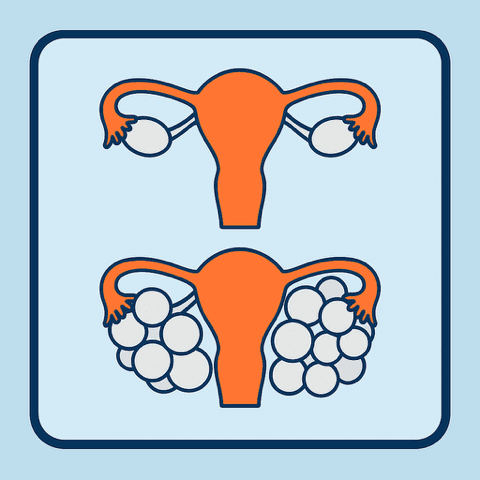
Fisiopatologia e Meccanismi Molecolari
La sindrome da iperstimolazione ovarica si sviluppa attraverso una cascata di eventi molecolari complessi che coinvolgono principalmente il sistema vascolare ovarico e la regolazione della permeabilità capillare. Il meccanismo principale è mediato dall'attivazione del recettore per l'ormone luteinizzante/gonadotropina corionica (LHCGR) da parte dell'hCG esogena somministrata per indurre la maturazione follicolare finale. Questa stimolazione prolungata, dovuta all'emivita estesa dell'hCG (circa 12 ore nella fase rapida), mantiene attivi i corpi lutei per un periodo di circa una settimana, determinando una produzione eccessiva di fattore di crescita endoteliale vascolare (VEGF). Il VEGF rappresenta il mediatore chiave nella patogenesi dell'OHSS, essendo una glicoproteina prodotta dalle cellule della granulosa ovarica che promuove la permeabilità vascolare, la proliferazione endoteliale e l'angiogenesi. L'aumento dei livelli di VEGF determina la caratteristica aumentata permeabilità capillare che consente il passaggio di fluidi ricchi di proteine dallo spazio intravascolare alle cavità corporee, generando il quadro clinico tipico dell'ascite e dell’idrotorace.
Classificazione Clinica e Presentazione Sintomatologica
La classificazione dell'OHSS si basa tradizionalmente sulla severità dei sintomi clinici e sui parametri laboratoristici, permettendo una stratificazione prognostica e terapeutica appropriata. Secondo le linee guida del Royal College of Obstetricians and Gynaecologists (RCOG) del 2016, la sindrome viene classificata in quattro gradi principali: lieve, moderata, severa e critica. Questa classificazione rappresenta un continuum di gravità che riflette l'evoluzione fisiopatologica della condizione e guida le decisioni terapeutiche.
L'OHSS lieve si caratterizza per lievi algie e distensione addominale, con volume ovarico inferiore a 8 cm. I pazienti possono presentare fastidio addominale di grado variabile, talvolta accompagnato da nausea, vomito o diarrea, con ovaie di volume aumentato evidenziabile all'esame ecografico. La forma moderata presenta moderata distensione addominale con volume ovarico compreso tra 8-12 cm, nausea con o senza vomito, e presenza di versamento addominale confermato mediante esame ecografico.
L'OHSS severa rappresenta una condizione clinica significativamente più grave, caratterizzata da versamento addominale confermato ecograficamente con possibile idrotorace associato, oliguria (meno di 30 ml/h o 300 ml/giorno), volume ovarico superiore a 12 cm, ematocrito maggiore di 0,45 e creatinina superiore a 1,6. I pazienti possono sviluppare compromissione respiratoria secondaria all'idrotorace e alla distensione addominale, richiedendo un monitoraggio clinico stretto e spesso il ricovero ospedaliero.
La forma critica dell'OHSS costituisce un'emergenza medica caratterizzata da evidenza clinica di ascite associata a uno o più dei seguenti segni: severo idrotorace, ematocrito superiore a 0,55, leucocitosi maggiore di 25.000/ml, oliguria o anuria (meno di 100 ml/giorno), fenomeni tromboembolici secondari all'emoconcentrazione, sindrome da distress respiratorio acuto, instabilità emodinamica con ipotensione ortostatica e tachicardia, ed emoperitoneo da rottura ovarica. Questa forma presenta un rischio significativo di mortalità e richiede gestione intensiva in ambiente ospedaliero specializzato.
Classificazione Temporale
Un'ulteriore classificazione dell'OHSS si basa sui tempi di insorgenza rispetto alla somministrazione di hCG, distinguendo forme precoci e tardive. L'OHSS precoce si manifesta entro 7 giorni dalla somministrazione di hCG ed è generalmente associata a un'eccessiva risposta alla stimolazione ovarica. Questa forma presenta tipicamente sintomi che si sviluppano 3-7 giorni dopo la somministrazione di hCG esogena, con il meccanismo patogenetico legato alla potenzializzazione del VEGF da parte dell'hCG. L'OHSS tardiva, invece, si presenta circa 12-17 giorni dopo la somministrazione iniziale di hCG e può essere correlata alla produzione endogena di hCG in caso di gravidanza.
Fattori di Rischio Identificati
I principali fattori di rischio per lo sviluppo di OHSS includono l'età giovane, la presenza di sindrome dell'ovaio policistico (PCOS), elevati livelli di ormone anti-Mülleriano, il pattern multifollicolare all'ecografia ovarica e precedenti episodi di OHSS. Altri fattori di rischio includono la risposta in cicli precedenti di stimolazione, il numero di follicoli sviluppati e i valori di estradiolo (E2) durante il ciclo di stimolazione. Il monitoraggio di questi parametri durante la stimolazione ovarica controllata è essenziale per identificare precocemente le pazienti a rischio e implementare strategie preventive appropriate. La gravidanza multipla e l'uso di protocolli di stimolazione aggressivi rappresentano ulteriori fattori che aumentano il rischio di sviluppare OHSS.
Diagnosi e Monitoraggio Clinico
La diagnosi di OHSS si basa su una combinazione di criteri clinici, laboratoristici e strumentali che permettono di identificare la condizione e di valutarne la severità. L'approccio diagnostico deve essere sistematico e multidisciplinare, coinvolgendo specialisti in medicina della riproduzione, radiologi e, nei casi più gravi, intensivisti. L'anamnesi deve focalizzarsi sui trattamenti di stimolazione ovarica recenti, sui sintomi sistemici e sulla progressione temporale della sintomatologia.
L'esame clinico riveste un ruolo centrale nella valutazione iniziale, con particolare attenzione alla presenza di distensione addominale, dolorabilità, segni di versamento peritoneale e alterazioni dell'equilibrio idroelettrolitico. La misurazione del peso corporeo e della circonferenza addominale rappresenta un parametro fondamentale per il monitoraggio dell'evoluzione della condizione, particolarmente importante per le pazienti gestite a domicilio. Il controllo della diuresi, sia in termini di frequenza minzionale che di volume urinario giornaliero, fornisce informazioni cruciali sulla funzione renale e sullo stato di idratazione.
Valutazioni Laboratoristiche
I parametri laboratoristici costituiscono elementi diagnostici e prognostici fondamentali nella gestione dell'OHSS. L'emocromo completo con particolare attenzione all'ematocrito e ai globuli bianchi fornisce informazioni sull'emoconcentrazione e su possibili complicanze infettive. L'ematocrito superiore a 0,45 indica emoconcentrazione significativa e definisce il passaggio dalla forma moderata a quella severa, mentre valori superiori a 0,55 caratterizzano la forma critica. La leucocitosi può essere presente come conseguenza dello stress sistemico, ma valori superiori a 25.000/ml definiscono la forma critica della sindrome.
La funzione renale deve essere monitorata attraverso la determinazione della creatinina sierica e la valutazione della clearance della creatinina. Valori di creatinina compresi tra 1,0-1,5 mg/dl indicano una compromissione funzionale renale moderata, mentre livelli superiori a 1,6 mg/dl definiscono la forma severa. Gli elettroliti sierici, in particolare sodio e potassio, devono essere controllati regolarmente per identificare precocemente squilibri che potrebbero richiedere correzione farmacologica. La valutazione degli enzimi epatici può rivelare disfunzione epatica associata, come documentato in casi di OHSS con transaminasi elevate.
Imaging Diagnostico
L'ecografia pelvica rappresenta l'esame strumentale di prima scelta per la diagnosi e il monitoraggio dell'OHSS, permettendo di valutare le dimensioni ovariche, la presenza di versamento peritoneale e le caratteristiche morfologiche dei follicoli. La classificazione ecografica distingue l'OHSS lieve (diametro ovarico < 5 cm con versamento < 3 cm senza ascite), moderata (diametro 5-12 cm con versamento di 3-6 cm e falda liquida nel Douglas) e severa (diametro > 12 cm versamento > 6 cm e ascite evidente). L'ecografia addominale può inoltre identificare la presenza di versamento libero peritoneale e quantificarne approssimativamente l'entità.
Nei casi più gravi, può essere necessario ricorrere a imaging avanzato come la tomografia computerizzata (TC) o la risonanza magnetica (RM) per valutare complicanze sistemiche, quantificare il versamento pleurico o identificare fenomeni tromboembolici. La radiografia del torace può rivelare la presenza di idrotorace, particolarmente importante per la valutazione della compromissione respiratoria nei casi severi e critici. L'ecocardiografia può essere utile per valutare la funzione cardiaca e lo stato volemico nei pazienti con instabilità emodinamica.
Gestione Terapeutica e Protocolli di Trattamento
La gestione dell'OHSS richiede un approccio stratificato basato sulla severità della condizione, con protocolli terapeutici differenziati che spaziano dal trattamento ambulatoriale conservativo per le forme lievi al ricovero in terapia intensiva per le forme critiche. L'obiettivo principale del trattamento è il mantenimento dell'equilibrio idroelettrolitico, la prevenzione delle complicanze sistemiche e il supporto della funzione d'organo compromessa. La gestione deve essere personalizzata in base alla presentazione clinica individuale e all'evoluzione della sintomatologia.
Per l'OHSS lieve-moderata, il trattamento può essere gestito a livello ambulatoriale con un protocollo di sorveglianza domiciliare strutturato. La terapia include analgesici orali per il controllo del dolore e counseling dettagliato riguardo la sorveglianza di segni e sintomi di peggioramento. È fondamentale evitare i rapporti sessuali, che potrebbero aumentare il rischio di rottura o torsione ovarica a causa dell'ingrandimento ovarico. L'attività fisica intensa deve essere evitata, ma è altrettanto importante prevenire l'allettamento prolungato per ridurre il rischio di fenomeni tromboembolici.
Protocollo di Monitoraggio Domiciliare
Il monitoraggio domiciliare per pazienti con OHSS lieve o moderata richiede l'adesione a un protocollo strutturato di auto-osservazione. Le pazienti devono misurare quotidianamente il peso corporeo e la circonferenza addominale per identificare precocemente segni di progressione della condizione. Il monitoraggio della frequenza minzionale e del volume urinario giornaliero fornisce informazioni cruciali sulla funzione renale e sullo stato di idratazione. È raccomandata l'esecuzione di prelievi venosi per emocromo (con particolare attenzione a globuli bianchi ed ematocrito), creatinina ed elettroliti ogni 3-4 giorni.
L'idratazione rappresenta un aspetto fondamentale della gestione, con raccomandazione di assumere non meno di 1 litro di acqua al giorno, preferibilmente sostituibile con bevande elettrolitiche per mantenere l'equilibrio idrosalino. Le pazienti devono essere istruite sui segni di allarme che richiedono immediata valutazione medica, inclusi peggioramento del dolore addominale, difficoltà respiratoria, riduzione significativa della diuresi, aumento rapido del peso corporeo o della circonferenza addominale. Un sistema di comunicazione efficace con il team medico deve essere stabilito per garantire interventi tempestivi in caso di deterioramento clinico.
Gestione dell'OHSS Severa e Critica
L'OHSS severa e critica richiede ricovero ospedaliero per garantire un monitoraggio clinico-strumentale stretto e interventi terapeutici intensivi. La gestione dei fluidi rappresenta l'aspetto più critico del trattamento, richiedendo uno stretto monitoraggio dei liquidi somministrati per via endovenosa e per via orale, bilanciati con quelli eliminati. Il trattamento inizia tipicamente con un bolo endovenoso di 500-1000 ml di fluidi, preferibilmente glucosata al 5% rispetto al ringer lattato, seguito da una cauta somministrazione per mantenere un output urinario adeguato (>20-30 ml/h) e ridurre l'emoconcentrazione.
La correzione dell'ipovolemia, dell'ipotensione e dell'oliguria ha la priorità assoluta, anche a discapito del potenziale peggioramento iniziale dell'ascite. Quando l'infusione di fluidi non risulta efficace nel correggere l'emoconcentrazione, è indicata la somministrazione di albumina umana al 25% in dosi di 50-100 g, ripetibile ogni 4-12 ore. I diuretici, in particolare la furosemide 20 mg endovena, devono essere considerati solo dopo aver raggiunto un ematocrito inferiore al 38%, per evitare un ulteriore peggioramento dell'ipovolemia.
Le complicanze elettrolitiche, in particolare l'iperpotassiemia, richiedono monitoraggio elettrocardiografico continuo e correzione farmacologica con calcio gluconato in presenza di alterazioni ECG caratteristiche (prolungamento PR e QRS, sottoslivellamento del tratto ST). La gestione delle complicanze respiratorie può richiedere supporto ventilatorio nei casi con severo idrotorace o sindrome da distress respiratorio acuto. La profilassi antitrombotica deve essere considerata in tutti i pazienti ospedalizzati data l'aumentata suscettibilità ai fenomeni tromboembolici.
Strategie di Prevenzione e Approcci Innovativi
La prevenzione dell'OHSS rappresenta l'approccio più efficace per ridurre la morbidità e mortalità associate a questa complicanza dei trattamenti di procreazione medicalmente assistita. Negli ultimi anni, l'evoluzione delle tecniche di stimolazione ovarica controllata e l'introduzione di nuovi protocolli farmacologici hanno permesso di sviluppare strategie preventive sempre più sofisticate ed efficaci. L'identificazione precoce dei fattori di rischio e l'utilizzo di approcci personalizzati rappresentano elementi chiave per la prevenzione primaria della sindrome.
Una delle innovazioni più significative nella prevenzione dell'OHSS è rappresentata dall'utilizzo di agonisti del GnRH per il triggering della maturazione follicolare finale, in sostituzione dell'hCG tradizionale. Questo approccio si basa sulla comprensione che l'hCG, con la sua emivita prolungata, mantiene attiva la stimolazione dei corpi lutei per circa una settimana, determinando una produzione eccessiva di VEGF. Al contrario, il triggering con agonisti del GnRH induce un rilascio endogeno di LH e FSH con una durata di circa 34 ore, più simile al surge gonadotropinico naturale che dura circa 48 ore.
Meccanismi di Azione degli Agonisti GnRH
Il meccanismo preventivo degli agonisti del GnRH si basa su molteplici effetti sinergici che riducono il rischio di sviluppare OHSS. Primo, la riduzione della durata della stimolazione delle cellule della granulosa/teca luteinizzate da giorni a ore diminuisce significativamente la produzione di VEGF. Secondo, l'induzione della luteolisi con rapida diminuzione dei livelli di estrogeni e progesterone contribuisce alla risoluzione precoce della stimolazione ovarica. Terzo, recenti evidenze suggeriscono che gli agonisti del GnRH possano aumentare direttamente l'espressione e la secrezione del fattore derivato dall'epitelio pigmentato (PEDF) da parte delle cellule della granulosa, che agisce come antagonista naturale degli effetti del VEGF sulla permeabilità vascolare ovarica.
L'effetto del PEDF rappresenta un meccanismo di protezione particolarmente innovativo, in quanto questo fattore può antagonizzare gli effetti avversi del VEGF sulla permeabilità vascolare ovarica e contribuire alla luteolisi riducendo la vascolarizzazione del corpo luteo. Questa scoperta apre nuove prospettive per lo sviluppo di strategie terapeutiche mirate che potrebbero includere l'utilizzo di agonisti della dopamina, che sembrano condividere meccanismi protettivi simili attraverso la stimolazione del PEDF.
Personalizzazione dei Protocolli di Stimolazione
La personalizzazione dei protocolli di stimolazione ovarica controllata rappresenta un approccio preventivo fondamentale basato sulla valutazione individuale dei fattori di rischio. I parametri attualmente utilizzati per prevenire l'insorgenza della sindrome includono il numero di follicoli sviluppati e i valori di estradiolo durante la stimolazione. Il monitoraggio ecografico seriale permette di identificare precocemente le pazienti che sviluppano un numero eccessivo di follicoli, consentendo l'implementazione di strategie preventive come la riduzione del dosaggio delle gonadotropine o l'annullamento del ciclo nei casi a rischio elevato.
L'utilizzo di biomarcatori predittivi come l'ormone anti-Mülleriano e il count dei follicoli antrali permette di stratificare il rischio prima dell'inizio della stimolazione e di personalizzare i protocolli farmacologici. Le pazienti ad alto rischio possono beneficiare di protocolli di stimolazione a basso dosaggio, dell'utilizzo di antagonisti del GnRH con triggering mediante agonisti, e di strategie di crioconservazione degli embrioni per evitare il transfer a fresco in presenza di rischio elevato di OHSS. Questi approcci personalizzati hanno dimostrato efficacia nel ridurre significativamente l'incidenza delle forme severe di OHSS mantenendo tassi di successo riproduttivo soddisfacenti.
Conclusioni
La sindrome da iperstimolazione ovarica rimane una delle complicanze più significative e potenzialmente pericolose associata ai trattamenti di procreazione medicalmente assistita, richiedendo un approccio multidisciplinare integrato che spazi dalla prevenzione primaria alla gestione delle forme critiche. L'evoluzione della comprensione fisiopatologica della condizione, centrata sul ruolo del VEGF e sui meccanismi di regolazione della permeabilità vascolare ovarica, ha permesso lo sviluppo di strategie preventive innovative particolarmente efficaci. L'introduzione del triggering con agonisti del GnRH rappresenta un avanzamento significativo nella prevenzione dell'OHSS, offrendo un'alternativa sicura ed efficace all'hCG tradizionale per le pazienti ad alto rischio.
La gestione terapeutica dell'OHSS richiede protocolli differenziati basati sulla severità della presentazione clinica, con particolare attenzione al mantenimento dell'equilibrio idroelettrolitico e alla prevenzione delle complicanze sistemiche. La personalizzazione dei protocolli di stimolazione ovarica, basata sulla valutazione individuale dei fattori di rischio e sull'utilizzo di biomarcatori predittivi, rappresenta l'approccio più promettente per la prevenzione primaria della sindrome.
Le prospettive future nella gestione dell'OHSS includono lo sviluppo di nuovi approcci farmacologici mirati ai meccanismi molecolari specifici, l'ottimizzazione dei protocolli di crioconservazione per ridurre la necessità di transfer a fresco in pazienti a rischio, e l'implementazione di sistemi di intelligenza artificiale per la predizione personalizzata del rischio. La formazione continua degli operatori sanitari e l'educazione delle pazienti sui fattori di rischio e sui segni di allarme rimangono elementi fondamentali per garantire una gestione ottimale di questa complessa condizione clinica. L'integrazione di queste strategie multidisciplinari promette di ridurre ulteriormente l'incidenza e la severità dell'OHSS, migliorando la sicurezza e l'efficacia dei trattamenti di procreazione
VUOI SAPERNE DI PIÙ?
Entra in contatto con noi e richiedi una consulenza con uno specialista della PMA
Altro in Approfondimenti
Hai ancora dubbi o semplicemente vuoi approndire altri argomenti sul mondo della procreazione medicalmente assitita? Consulta i nostri articoli, troverai spunti interessanti che sapranno dare risposta ad ogni tua perplessità.